| De nouveaux espoirs contre les bactéries pathogènes |
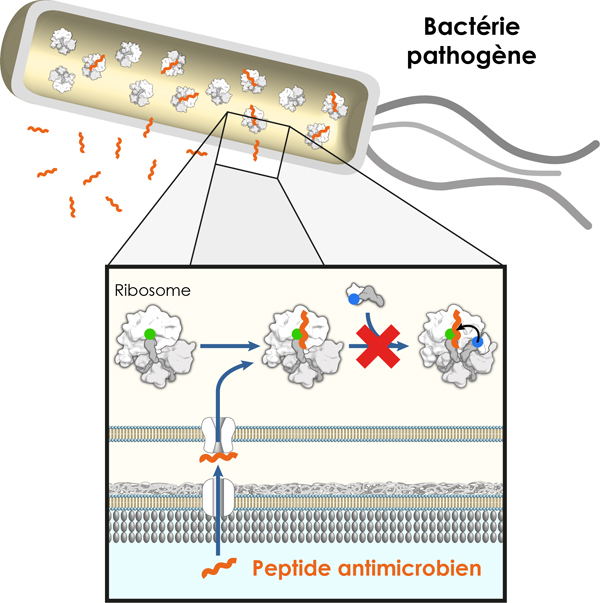
De nouveaux espoirs contre les bactéries pathogènes Deux équipes de l’IECB, en collaboration avec une équipe de recherche de l’Université de Munich, viennent de caractériser des peptides antimicrobiens qui pourraient servir de base au développement de nouveaux antibiotiques. Des résultats qui viennent d’être publiés dans la revue Nature Structural and Molecular Biology.
Pour éliminer les bactéries, les antibiotiques ont la capacité à bloquer de manière spécifique des processus essentiels à leur survie, telles que la synthèse de la paroi cellulaire, la réplication du matériel génétique ou la synthèse des protéines par le ribosome. Ce dernier est la cible privilégiée pour plus de la moitié des antibiotiques actuellement disponibles sur le marché. Dans le cadre de cette collaboration internationale, les chercheurs ont démontré comment l’oncocine, un peptide antimicrobien produit par le système immunitaire de certains insectes, parvient à inhiber de manière spécifique la synthèse des protéines par le ribosome bactérien. Dans un premier temps l’équipe du Dr. Axel Innis (IECB – Inserm U869) a obtenu par diffractométrie à rayons X la structure atomique précise de l’oncocine en complexe avec le ribosome de la bactérie Thermus thermophilus*. Des résultats biochimiques complémentaires ont été obtenus par l’équipe du Dr. Daniel Wilson (Université de Munich) avec des analogues de l’oncocine comprenant différentes mutations, dont certains acides aminés non naturels, synthétisés par l’équipe de chimie peptidomimétique du Dr. Gilles Guichard (IECB – CNRS UMR5248). Ces travaux ont montré que l’oncocine interagit avec un long tunnel ribosomal par lequel les protéines nouvellement synthétisées rejoignent le milieu intracellulaire. Une fois ancré dans le tunnel, le peptide masque le site actif du ribosome, empêchant ainsi la bactérie de synthétiser des protéines. Le site d’interaction entre l’oncocine et le tunnel coïncide par ailleurs avec des régions du ribosome ciblées par de nombreux antibiotiques, soulignant l’intérêt de ces résultats pour le développement de futurs composés antimicrobiens. Ces résultats ont été publiés le 18 mai 2015 dans la revue Nature Structural and Molecular Biology.
*: Thermus thermophilus est une bactérie dite à Gram-négatif. Les bactéries à Gram-négatif pathogènes constituent un problème majeur pour les hôpitaux, maisons de retraite et autres établissements de santé (bactéries telles que Klebsiella, Pseudomonas ou Acinetobacter) où elles provoquent des infections souvent difficiles à traiter chez les personnes âgées ou gravement malades. |
2, Rue Robert Escarpit - 33607 PESSAC - France
Tel. : +33 (5) 40 00 30 38 - Fax. : +33 (5) 40 00 30 68